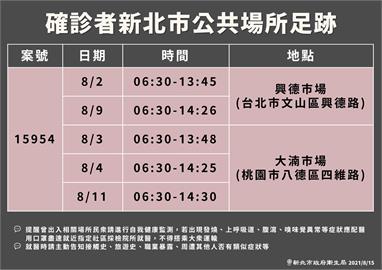
南韓政府日前正式通過《SK Bioscience》國產疫苗「GBP510」的第3期臨床實驗,將採免疫橋接方式,與阿斯特捷利康(AZ)疫苗進行抗體濃度比對,最快可望明年初上市。不過SK的國產疫苗在未來還得面臨層層考驗,包括能否通過國際認證、在銷售市場上與mRNA疫苗的競爭、能否對抗變種病毒。
《SB Bioscience》日前發布新聞稿,表示南韓研發的國產疫苗主要是利用重組蛋白技術,第3期的臨床試驗將採免疫橋接的方式進行,這種方式是繼法國Valneva的國產疫苗VLA2001後,全球第2支採用免疫橋接進行的疫苗。
《SB Bioscience》發布的新聞稿表示,日前南韓政府已則批准了SK生物科學的GBP510新冠疫苗進行第三期臨床試驗,《SB Bioscience》也表示第三期結果的分析將在明年第一季出爐,並盡力爭取在2022上半年實施商用化。
根據南韓媒體《中央日報》指出,GBP510為「重組蛋白疫苗」,是用基因重組技術製作病毒表面的棘狀蛋白,注射進入人體後、刺激免疫細胞產生抗體,與我國的高端、聯亞,美國的Novamax疫苗類似。但《韓聯社》指出,其實GBP510的二期臨床還在進行當中,但其一期臨床結果顯示,所有接種者產生中和抗體,血清檢出率高於治癒病例的5倍以上,且沒有異常反應報告,安全性和免疫原性也得到驗證。
(民視新聞網/綜合報導)